Введение
Кость — это орган, являющийся компонентом системы органов опоры и движения, имеющий типичную форму и строение, характерную архитектонику сосудов и нервов. Костная ткань на 2/3 состоит из минеральных соединений, главным образом из солей кальция в форме гидроксиапатитных кристаллов и органического матрикса, который на 90% представлен коллагеном I типа. Ведущая роль в формировании костной системы принадлежит макро- и микроэлементам. Значительное влияние среди макроэлементов имеет кальций, магний и фосфор. Их дефицит может приводить к нарушению как формирования, так и резорбции костной ткани.
Большинство регуляторных механизмов направлено на процессы резорбции костной ткани. Ключевую роль в понимании процессов регуляции костной реконструкции принадлежит цитокиновой системе рецептора активатора ядерного фактора каппа-B (RANK), его лиганда (RANKL) и остеопротегерина (OPG) [1], отвечающей за остеокластогенез, резорбцию и ремоделирование костной ткани. Открытие данной системы в 1997 г. помогло понять патогенез остеопороза (ОП), остеокластогенеза, регуляцию костной резорбции, локальных процессов репарации.
Регуляция ремоделирования костной ткани происходит под действием паратиреоидного гормона (ПТГ), 1,25-дигидроксивитамина D3 и кальцитонина на уровне органов-мишеней — кишечника, почек и костной системы. Любое снижение концентрации кальция в сыворотке крови приводит к развитию вторичного гиперпаратиреоза, для поддержания физиологического уровня кальция, необходимого для нормального клеточного метаболизма [2]. Центральная роль в поддержании гомеостаза кальция в организме и здоровья костей принадлежит витамину D3, а данные, указывающие на взаимосвязи уровня витамина D3 при различных хронических заболеваниях по-прежнему определяют интерес к данной проблеме. Витамин D3 — холекальциферол синтезируется в мальпигиевом слое эпидермиса из 7-дигидрохолестерина под действием УФО спектра 290–315 нм. Холекальциферол гидроксилируется в печени, образуя 25-гидроксивитамин D3. Последний не обладает никакой метаболической активностью и только после последующего гидроксилирования в почках под влиянием ПТГ синтезируется в активную форму 1,25-дигидроксивитамина D3 — кальцитриол, обеспечивающий и поддерживающий гомеостаз кальция через его регуляцию в кишечнике и костях.
ОП — системное заболевание скелета, характеризующееся снижением костной массы и микроструктурной перестройкой костной ткани, приводящими к повышенной хрупкости кости. Вследствие снижения костной массы при ОП происходят переломы как при незначительной травме, так и при статической нагрузке. Прочность кости отражает интеграцию двух главных характеристик костной ткани: минеральной плотности и качества кости (архитектоника, обмен, накопление повреждений, минерализация)
ОП в настоящее время самое распространенное метаболическое заболевание опорно-двигательного аппарата, для которого характерно снижение костной массы в единице объема, что происходит постепенно, скрыто и часто выявляется после переломов позвонков, шейки бедренной кости, проксимального отдела лучевой кости и других локализаций.
Результаты проведенного анализа данных Российской ассоциацией по остеопорозу в 2010 г. [3] показали, что население России составило 142 млн человек, из них 45,5 млн (32%) — люди в возрасте 50 лет и старше. При этом средняя продолжительность жизни женщин значительно выше, чем у мужчин (72 года против 59 лет). Таким образом, на настоящий момент в Российской Федерации ОП страдают 14 млн человек (10% населения страны), у 20 млн есть остеопения. Ожидается, что к 2020 г. в Российской Федерации количество лиц в возрасте 50 лет и старше увеличится до 48 млн человек, а к 2050 г. до 56%, а в возрасте 70 лет и старше — до 20%, что предполагает увеличение числа больных ОП на 1/3.
Влияние внешних факторов на минеральный обмен костной ткани
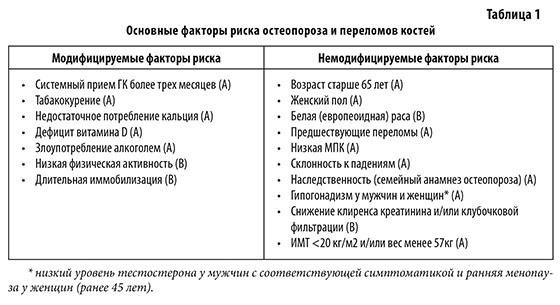
Костная масса нарастает до 25–30 лет и после завершения роста у остается практически неизменной. В периоде старения резорбция начинает преобладать над синтезом кости, что приводит к снижению костной массы. Считается, что уровень костной массы в пожилом возрасте зависит от двух факторов — массы кости, сформированной в подростковом периоде и скорости костной резорбции в процессе старения. На величину костной массы влияют генетический статус, физическая активность и алиментарный фактор. Скорость потери костной массы определяется большим количеством факторов, такими как: недостаток половых гормонов (менопауза, оофрэктомия, аменорея, гипогонадизм), возрастные изменениями (снижение физической активности, всасывания кальция в желудочно-кишечном тракте). Кроме того, снижение костной массы может быть следствием хронических заболеваний (эндокринных, ревматических, гематологических гастроэнтерологических, нефрологических, алкоголизма) или лекарственной терапии, прежде всего, глюкокортикоидной. При ОП необходимо целенаправленное выявление пациентов с факторами риска ОП и переломов с целью профилактики либо формирования групп риска для последующего обследования и лечения ОП (табл. 1).
Среди внешних факторов риска ОП особую роль занимает влияние экстремальных условий Севера. Как известно, около 70% России занимают Северные территории, что определяет актуальность проблемы. В условиях Севера, по-прежнему остается одной из самых актуальных проблема минерального обмена костной ткани. К факторам, вызывающим данные изменения относятся: низкая температура среды, специфическая для этих широт фотопериодичность, высокая ионизация воздуха и резкие непериодические колебания напряжения геомагнитного и статического электрического поля, перепады атмосферного давления, низкая парциальная плотность кислорода в воздухе. Неблагоприятное воздействие на организм перечисленных факторов приводит к развитию сдвигов основных физиологических процессов, формированию «полярного» метаболического типа обмена. Помимо неблагоприятного влияния природно-климатических условий, отрицательное воздействие могут оказывать такие модифицированные факторы как курение, гиподинамия, недостаточное потребление кальция, злоупотребление алкоголем.
Установлено, что у лиц, проживающих в условиях Севера, наблюдается чаще снижение минеральной плотности костной ткани (МПКТ), чем в других регионах. По данным многоцентрового межнационального исследования MEDOS [4], показано увеличение частоты переломов проксимальных отделов бедренной кости, преимущественно в северных регионах Европы.
В многочисленных исследованиях, рассматривающих влияние сезонности на МПКТ, показано, что наименьший уровень в сыворотке крови витамина D3 наблюдается преимущественно в зимнее время — декабрь–февраль. По результатам ряда исследований снижение уровня витамина D3 совпадает со значительным усилением минерального обмена костной ткани, однако есть работы не подтверждающие данный факт.
До сих пор остается дискутабельным вопрос об оптимальном содержании витамина D3 в сыворотке крови. Многие исследователи определяют необходимое содержание витамина D3 как самую низкую концентрацию в сыворотке крови D3, максимально подавляющую секрецию ПТГ и оптимизирующую МПКТ. На основании этих критериев, большинство экспертов полагают, что уровень витамина D3 от 21 до 30 нг/мл свидетельствуют относительной недостаточности, в то время как уровень менее 20 нг/мл является дефицитом витамина D3. По данным доклада Американского института медицины, опубликованного в 2011 г., уровень витамина D3 является адекватным, когда он равен или выше 50 нмоль/л. Недавние исследования показали, что минимальный пороговый уровень D3, необходимый для профилактики разрушения кости, составляет 29,7 нг/мл [5]. Однако, есть определенная проблема в отношении оптимальной концентрации витамина D3 для профилактики переломов. Витамин D3 обладает рядом внескелетных действий, включая укрепление иммунитета, профилактику рака и артериальной гипертензии. В связи с этим доза витамина D3, необходимая для реализации данных эффектов может быть значительно выше, чем необходимо для обеспечения адекватного метаболизма костной ткани.
Диагностика ОП
Для диагностики ОП в настоящее время широко используется рентгенография и двухэнергетическая рентгеновская абсорбциометрия (DEXA).
Рентгендиагностика является первым лучевым методом для выявления ОП. Выделяют следующие рентгенологические признаки ОП позвоночника (H. P. Kruse, 1978):
- снижение плотности рентгенологической тени;
- истончение поперечных трабекул и кортикального слоя, подчеркнутость замыкательных пластин;
- дальнейшая атрофия трабекулярного рисунка, дополнительный вертикальный акцент губчатого слоя тел позвонков;
- деформация позвонков (клиновидная, двояковогнутая, деформация сдавления).
 В настоящий момент в ВС Российской Федерации рентгенологическая оценка по-прежнему остается единственным доступным и распространенным методом визуализации ОП. Рентгенография позволяет определять локализацию снижения МПКТ лишь в том случае, когда потеря костной ткани достигает значительных величин — 20–50%, что снижает значение данного метода для ранней диагностики ОП. Рентгенография необходима для обнаружения уже имеющихся деформаций, переломов или трещин
В настоящий момент в ВС Российской Федерации рентгенологическая оценка по-прежнему остается единственным доступным и распространенным методом визуализации ОП. Рентгенография позволяет определять локализацию снижения МПКТ лишь в том случае, когда потеря костной ткани достигает значительных величин — 20–50%, что снижает значение данного метода для ранней диагностики ОП. Рентгенография необходима для обнаружения уже имеющихся деформаций, переломов или трещин
Денситометрия на сегодняшний день является наиболее распространенным и достоверным методом измерения МПКТ с целью диагностики ОП на ранних стадиях, обеспечивающим при минимальной лучевой нагрузке визуализировать от 2 до 5% потери МПК. Точность исследования превосходит ультразвуковое, не уступая при этом компьютерной томографии.
Лабораторная диагностика ОП включает определение маркеров костеобразования и резорбции костной ткани.
Маркеры костеобразования:
- остеокальцин (синтезируемый остеобластами),
- костный изофермент щелочной фосфатазы;
- карбокситерминальные пропептиды проколлагена 1 типа.
Маркеры резорбции костной ткани:
- продукты деградации коллагена 1 типа:
- -N- и С-телопептиды молекул коллагена I типа (NTX, CTX) в крови и моче
- оксипролин (OHPr)*;
- оксипиридинолин (PYR)*;
- дезоксипиридинолин (DPYR)*;
- тартрат-резистентная кислая фосфатаза (TRACP).
Маркеры костного ремоделирования (резорбции при назначении антирезорбтивной терапии и костеобразования при назначении анаболической терапии) рекомендовано определять исходно и через 3 месяца от начала терапии с целью ранней оценки эффективности лечения и приверженности к терапии. Достаточно оценивать один маркер, но одним и тем же лабораторным набором.
Лечение
Обязательной частью лечения ОП является немедикаментозная терапия:
- ходьба и физические упражнения (упражнения с нагрузкой весом тела, силовые упражнения и тренировка равновесия);
- прыжки и бег противопоказаны;
- коррекция питания (продукты, богатые кальцием) (D);
- отказ от курения и злоупотребления алкоголем (D);
- образовательные программы («Школа здоровья для пациентов с остеопорозом») (В);
- ношение жестких и полужестких корсетов для снижения выраженности болевого синдрома после перелома позвонка (А). Длительное ношение корсета может привести к
- слабости мышц спины и, как следствие, к плохим отдаленным результатам (D);
- постоянное ношение протекторов бедра пациентами, имеющими высокий риск развития перелома проксимального отдела бедра и имеющими факторы риска падений (В);
- у пациентов с ОП переломом позвонка и хронической болью в спине возможно применение кифопластики и вертеброплатики для уменьшения болевого синдрома,
- коррекции осанки и уменьшения риска последующих переломов (C);
- мануальная терапия при остеопорозе позвоночника противопоказана в связи с высоким риском переломов позвонков (D);
- при высоком риске падений — мероприятия, направленные на снижение риска падений (D);
- лечение сопутствующих заболеваний, коррекция зрения, коррекция принимаемых медикаментов, оценка и изменение домашней обстановки (сделать ее более безопасной), обучение правильному стереотипу движений, пользование тростью, устойчивая обувь на низком каблуке, физические упражнения на координацию и тренировку равновесия.
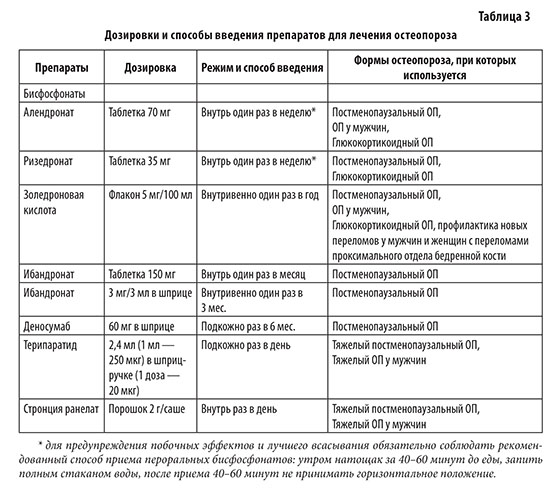
Медикаментозная терапия. При лечении женщин в постменопаузе и мужчин 50 лет и старше с ОП в настоящее время используются азотсодержащие бисфосфонаты (алендроновая, ризедроновая, ибандроновая, золедроновая кислоты), деносумаб, тирепаратид и стронция ранелат.
Заключение
ОП в настоящее время входит в число наиболее распространенных заболеваний, что обусловлено не только старением населения, приводящим к высокой инвалидизации и смертности пациентов, но и омоложением болезни, что отражено в клинических рекомендация по диагностике, профилактике и лечению ОП. Несмотря на общепринятое мнение о преимущественном распространении ОП у женщин, что подтверждается высокой частотой переломов проксимального отдела бедра и костей предплечья, показано что частота переломов позвонков у мужчин такая же, как и у женщин. Данный факт объяснятся анатомическими особенностями костной ткани и темпами потери костной массы.
Метод DEXA, позволяющий диагностировать снижение МПКТ на ранних этапах, не получил массового распространения в Российской Федерации. Недостаток рентгеновских костных денситометров и их сконцентрированность в крупных городах, приводит к запоздалой диагностике и как следствие отсутствию адекватной профилактики остеопоротических переломов.
Литература
1. Walsh M. C., Choi Y. Biology of the RANKL–RANK–OPG System in Immunity, bone and Beyond // Inflammation. 2014. Vol. 5. P. 511 [Электронный ресурс]. URL: www.ncbi.nlm.nih.gov/pmc/articles/PMC4202272/ (дата обращения: 11.01.2020).
2. Adams J. S. Update in vitamin D / J.S Adams, M. Hewison // J. Clin. Endocrinol. Metab. 2010. Vol. 95. N 2. P. 471–478.
3. Лесняк О. М. Аудит состояния проблемы остеопороза в Российской Федерации // Профилакт. медицина. 2011. Т. 14. № 2. С. 7–10.
4. Elffors I., Allander E., Kanis J. A. et al. The variable incidence of hip fracture in southern Europe: the MEDOS Study ander // Osteoporosis Int. 1994. Vol. 4. N 5. P. 253–263.
5. Khazai N., Judd E., Tangpricha V. Calcium and vitamin D: skeletal and extraskeletal health // Curr. Rheumatol. Rep. 2008. Vol. 10. N 2. P. 110–117.



