 Александр Григоьевич ЧУЧАЛИН,
Александр Григоьевич ЧУЧАЛИН,
академик РАН, профессор, заведующий кафедрой госпитальной терапии Российского национального исследовательского медицинского университета им. Н. И. Пирогова
Исторические аспекты
Коронавирус — инфекция, имеющая давнюю историю. Однако открытие его приходится только на 1931 г., когда в практику исследований пришел электронный микроскоп. События, которые предшествовали открытию коронавируса, были связаны с тотальной гибелью от непонятной инфекции цыплят на птицеферме. С помощью электронной микроскопии американским ветеринарам A. F. Schalk и M. C. Hawn тогда впервые удалось идентифицировать вирус, который впоследствии назвали коронавирусом птиц (ACoV — Avian coronavirus) [1]. Получить изолированный вирус не удавалось до 1965 г., когда D. A. Tyrrell и M. L. Bynoe, сотрудники отдела острых респираторных заболеваний Медицинского госпиталя в г. Солсбери (Великобритания), выделили его на культуре клеток эмбриональной трахеи (биологическая клетка-мишень коронавируса — эпителиальная клетка) и получили штамм первого коронавируса человека (HCoV — Human coronavirus) [2].
| Научное название Coronavirus было принято в качестве названия рода Международным комитетом по номенклатуре вирусов (позже переименованным в Международный комитет по таксономии вирусов) в 1971 г. [3]. По мере увеличения числа новых видов род был разделен на четыре рода: Alphacoronavirus, Betacoronavirus, Deltacoronavirus и Gammacoronavirus в 2009 г. Общее название «коронавирус» используется для обозначения любого члена подсемейства Orthocoronavirinae. По состоянию на 2020 г. официально признано 45 видов. |
На протяжении значительного периода времени к коронавирусам относились как к легким простудным формам, они считались безопасными для человека. Отмечалось, что коронавирус, как правило, действует в ассоциации с другими возбудителями, кроме гриппа. Обращала на себя внимание связь риновирус-коронавирус, часто приводившая к обострению бронхиальной астмы. Длительное время считалось, что грипп и коронавирус не ассоциируют. Однако осень 2022 г. перечеркнула это представление. На сегодняшний день произошло смешение, появилась микст-инфекция — это коронавирус, вирусы гриппа H1N1, Н3N2. Кроме того, отмечались локальные вспышки Крымской геморрагической лихорадки [4]. Частота диагностирования среди популяции инфекций, связанных с респираторно-синцитиальным вирусом, на октябрь 2022 г. составляла 15–20% [5].
Итак, в самом начале XXI в., до 2002 г., к коронавирусу относились как просто к простудному заболеванию. Мир полагал, что существует четыре сезонных коронавируса. Что же произошло в 2002 г.? Вирус тяжелого острого респираторного синдрома (SARS-CoV — Severeacute respiratory syndrome-related coronavirus) (Betacoronavirus, Sarbecovirus) был идентифицирован как этиологический агент эпидемии в южных провинциях Китая. Было установлено, что заражение людей произошло от животных семейства виверровых — гималайских цивет.
В 2012 г. началась история изучения вируса Ближневосточного респираторного синдрома (MERS-CoV — Middle East respiratory syndrome-related coronavirus) (Betacoronavirus, Merbecovirus). В сентябре 2012 г. в одну из лондонских клиник поступил 49-летний мужчина с внебольничной двусторонней пневмонией. Он был доставлен из госпиталя Катара, до этого посещал Саудовскую Аравию и скончался на 30 сутки от начала заболевания. Из трахеальных аспиратов пациента был выделен штамм MERS-CoV. Серологическая разведка в популяциях сельскохозяйственных животных на территории Омана показала, что 100% одногорбых верблюдов (Camelus dromedarius) имеют антитела против субъединицы S1 спайкового белка MERS-CoV. В дальнейшем были получены прямые доказательства циркуляции в организме верблюдов вариантов MERS-CoV, идентичных эпидемическим, и возможности заражения человека от этих животных [6].
В начале декабря 2019 г. в срединной китайской провинции Хубэй стали развиваться эпидемические события, связанные с новым коронавирусом, способным вызывать у людей тяжелые (вплоть до летальных) первичные вирусные пневмонии. Первый случай такой пневмонии был официально зарегистрирован в городе Ухань. Вскоре изолированный этиологический агент заболевания был идентифицирован как представитель Coronaviridae и получил временное обозначение 2019-nCoV [6].
Имеет ли отношение человек к появлению этих разновидностей коронавирусов? Отвечая на этот вопрос, можем вспомнить о точке зрения В. И. Вернадского, занимавшегося проблемами биосферы, согласно которой человек осуществляет на земле масштабные преобразования, сопоставимые с геологическими процессами. Можно сказать, что эпидемиологический кризис обусловлен деятельностью человека, поскольку так или иначе заражение коронавирусом происходит с участием животных, которых люди в ходе своей экономической деятельности разводят на фермах, используют в пищевой, парфюмерной и др. промышленностях.
Эпидемология
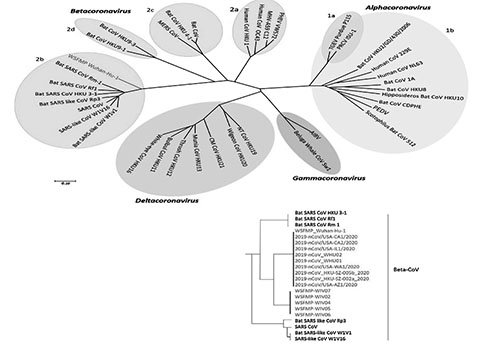
Коронавирус в XXI в. быстро прирастает все новыми разновидностями. Сегодня его филогенетическое дерево представлено более 50 серотипами (рис. 1).
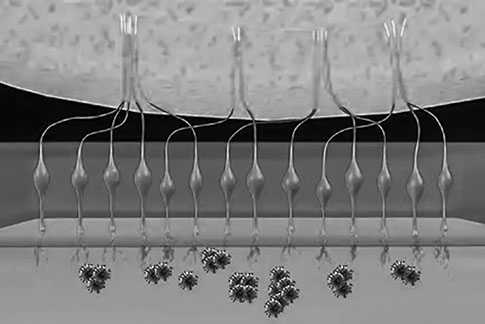
Что происходит при заражении? Короткий инкубационный период, который распространяется на первые дни инфицирования, заканчивается репликацией вируса в эпителиальных клетках слизистой носа. Биологической мишенью являются клетки нейроэпителия полости носа (рис. 2), на апикальной части которых имеется высокая плотность ангиотензинпревращающего фермента 2 (АПФ2). На этом этапе пациенты зачастую отмечают потерю обоняния, что отражает нейровоспалительный процесс, в который вовлекается nervus olfactorius. У некоторых пациентов наблюдаются изменения вкусовых восприятий, что может быть связано с воспалительным процессом вкусовых луковиц nervus vagus, nervusglossopharyngeus.
После внедрения вируса в организм через верхние дыхательные пути и стадии экспоненциального размножения вирусных частиц биологической мишенью для SARS-CoV становится дистальный отдел дыхательных путей, альвеоциты 2-го типа. Так же, как и нейроэпителий полости носа, альвеоциты 2-го типа имеют высокую плотность рецепторов АПФ2. Это следующий критический этап заболевания. В момент контакта вирусных частиц с данными рецепторами у больного поднимается температура, а также возникает кашель — астмоподобный, сухой, непродуктивный. При этом страдает и нереспираторная функция легких, имеющая иммунологические аспекты, а также нарушается метаболическая активность. Кроме того, повреждается альвеолокапиллярная мембрана, страдает газообмен, кислород перестает поступать в капиллярное ложе, нарушается процесс диссоциации и развивается гипоксемия. Таким образом, стадия вирусемии характеризуется сильной лихорадкой, сухим кашлем, дыхательным дискомфортом. В дальнейшем возможны два сценария: может возникнуть «окно», на котором процесс закончится, или же процесс перейдет в последующие осложнения, которые затронут такие важные функции, как газообмен легочной ткани, вследствие чего разовьется респираторный дистресс-синдром и т. д.
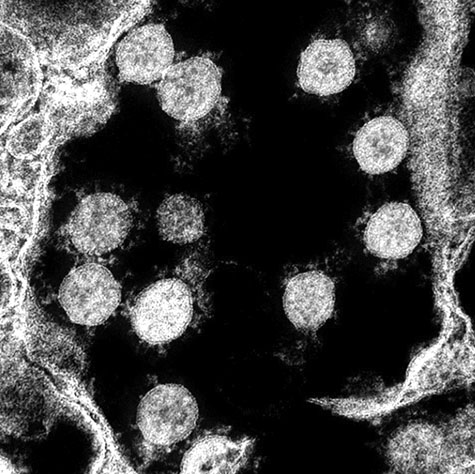
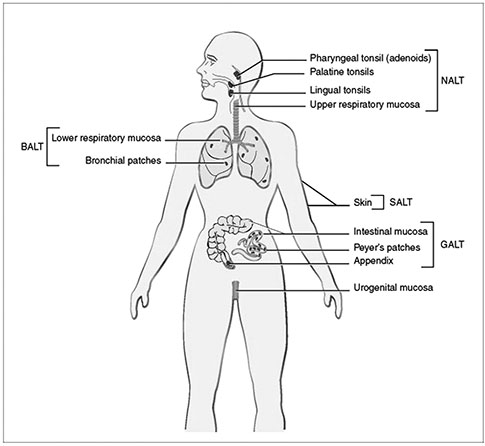
| Рис. 3. Вирус SARS-CoV-2 под электронным микроскопом [8] | Рис. 4. Мукозоассоциированная лимфоидная ткань (MALT) [9] |
Коронавирусная инфекция приводит к резкому нарушению мукозального иммунитета (иммунитета слизистых, кожи, барьерных тканей), включающего как врожденный (неспецифический) иммунитет, так и приобретенный (специфический или адаптивный) иммунитет. Стремительная репликация SARS-CoV-2 происходит в условиях супрессии мукозального иммунитета. Известно, что иммунитет слизистых оболочек реализуется через единую структурированную и высокоспециализированную систему — мукозоассоциированную лимфоидную ткань (mucosa-associated lymphoid tissue — MALT), состоящую из специализированных эпителиальных клеток, лимфоидных структур и иммунных молекул, расположенных в подслизистой основе. MALT —многоуровневая система, в которой выделяется лимфоидная ткань, ассоциированная с носоглоткой, трахеей, гастроинтестинальной системой, урогенитальным трактом и др.
Основным фактором защиты на уровне слизистых оболочек является секреторный IgA, который синтезируется в субэпителиальной части слизистых оболочек дыхательных путей и желудочно-кишечного тракта (рис. 5). Антитела секреторного IgA эффективны против различных видов патогенов, включая вирус SARS-CoV. Существующие вакцины в основном оказывают иммуностимулирующий эффект на приобретенный иммунитет. В настоящее время ведутся научные разработки вакцин для регуляции врожденного и мукозального иммунитета.

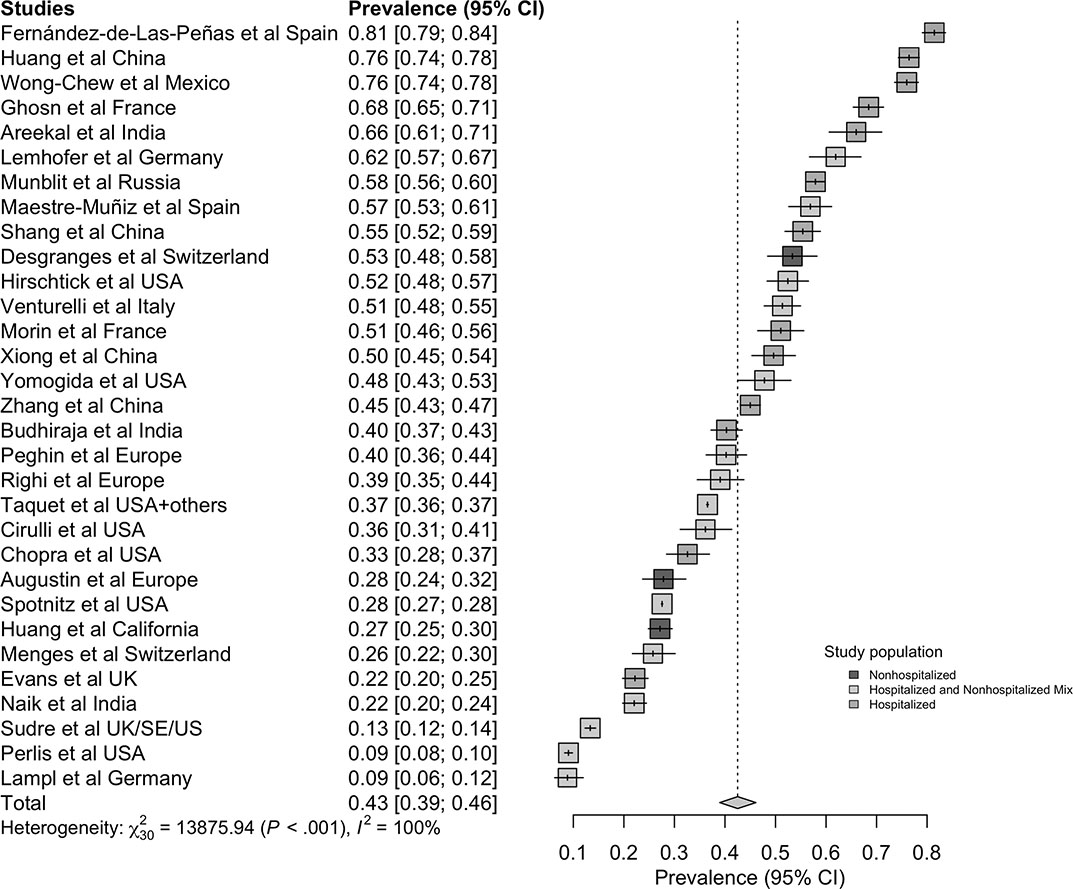
| Рис. 5. Солитарные (одиночные) лимфоидные фолликулы | Рис. 6. Результаты анализа мировых данных о распространенности постковидного синдрома в 2019 г. [10] |
Однако до сих пор мы не сильны в определении постковидного синдрома. Неоднозначность данных по эпидемиологии постковидного синдрома связана со многими причинами, включая отсутствие четких диагностических критериев, различность подходов к оценке симптомов, к серологическим исследованиям, к оценке тяжести последствий данного синдрома. На рис. 6 показаны данные, опубликованные C. Chen в 2022 г., демонстрирующие значительный разброс показателя распространенности постковидного синдрома у различных исследователей в различных странах, что свидетельствует об отсутствии единого понимания.
Так, в исследованиях, проведенных в Азии, распространенность постковидного синдрома составляла 0,51 [0,37–0,65], в Европе — 0,44 [0,32–0,56], в США — 0,31 [0,21–0,43]. Для всех исследований в целом этот показатель характеризуется значениями 0,43 [0,39–0,46]. У мужчин он составляет 0,37 [0,24–0,51], у женщин — 0,49 [0,35–0,63]. Для негоспитализированных пациентов — 0,34 [0,25–0,46], для госпитализированных — 0,54 [0,44–0,63]. Постковидный синдром встречается, огрубленно, у каждого второго человека, перенесшего острое инфекционное заболевание, вызванное SARS-CoV-2.
По данным Azzolini, 2022 г. и Byambasuren, 2022 г., распространенность постковидного синдрома у невакцинированных больных составила 41,8% [37–46,7%], после первой вакцинации — 30% [6,7–65,2%], после второй — 17,4% [7,8–31,4%], после третьей — 16% [11,8–21%] [11, 12]. Предварительные результаты систематического обзора показали, что три вакцины представляют собой стратегию, направленную на ослабление действия короновирусной инфекции, включая и те новые штаммы, которые появляются.
Патобиология постковидного синдрома
Постковидный синдром имеете три наиболее важных компартмента:
- сохранение вирусного резервуара;
- вовлечение аутоиммунных процессов;
- замедленное разрешение воспалительного процесса.
Важным патогенетическим звеном у пациентов с COVID-19 является гибель эндотелиоцитов. Вирусные частицы убивают эндотелиоциты, вызывая резкие морфологические изменения, в результате которых клетка превращается в перфорированную субстанцию, не имеющую своей архитектуры. Капилляры, венулы — «колено», где эндотелиоциты синтезируют фактор Виллебранда, играющий ключевую роль в предотвращении тромбообразования. Утрата эндотелиоцитами способности продуцировать фактор Виллебранда приводит к образованию микротромбов — микроэмболов. Гиалуроновая кислота играет вторичную роль, поддерживая коагулопатию. Преодолеть с помощью искусственной вентиляции легких тромбообразующие эффекты микроциркуляции невозможно.
Говоря о ковиде, следует вспомнить замечательную работу ученика С. П. Боткина Эдуарда Изаксона «О патолого-анатомических изменениях легочных сосудов при эмфизематозном процессе в легких». Э. Изаксон стремился понять природу эмфиземы легких, он считал, что эмфизема у человека образуется за счет облитерации капилляров. В своей работе Изаксон использовал собственные зарисовки (рис. 7).
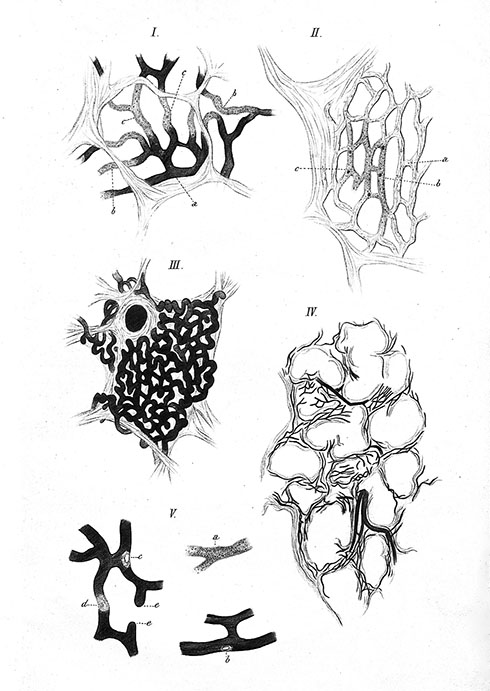 |
Рис. 7. Рисунки Э. Изаксона к диссертационной работе «О патолого-анатомических изменениях легочных сосудов при эмфизематозном процессе в легких». I — эмфизематозное легкое, инъецированное окрашенной массой: a — нормальные капилляры, b — зернисто-измененные сосуды, c — капиллярный тромб; II — эмфизематозное легкое, инъецированное серебряным раствором: a — петля нормальных капилляров, b — капиллярный тромб, c — зернисто-измененные сосуды; III — здоровые легочные сосуды, инъецированные крашенной массой; IV — легочные сосуды эмфизематозного легкого, инъецированные крашенной массой; V: a — измененный капилляр, |
В своем исследовании ученый писал: «капиллярный тромб есть ближайшая причина атрофии легочной ткани». Так появилась сосудистая теория эмфиземы.
Сегодня технология капилляроскопии очень бурно развивается. Она позволяет определить многие параметры: диаметры венул, капилляров, линейную скорость, объемную скорость, соотношение жидкостей перикапиллярной области и т. д. Таким образом открываются широкие перспективы для исследования микроциркуляции. Использование видеокапилляроскопии ногтевого ложа у пациентов после COVID-19 позволяет выявить патологические изменения капиллярного русла (расширенные капилляры, извилистые капилляры и низкую плотность капиллярной сети). Применение метода бульбарной капилляроскопии позволяет проводить детальную оценку всех звеньев микроциркуляторного русла.

Рис. 8. Эндотелиоциты в крови, взятой из кубитальной вены: а — эндотелиальные клетки больного COVID-19
с характерными отверстиями на мембране; б — отверстие в мембране той же клетки, соответствующее размеру
суперкапсида вируса SARS-CoV-2 (ув. 103 тыс.); в, д — при поступлении в больницу; д, е, ж — при выписке (ув. 10 тыс.) [13]
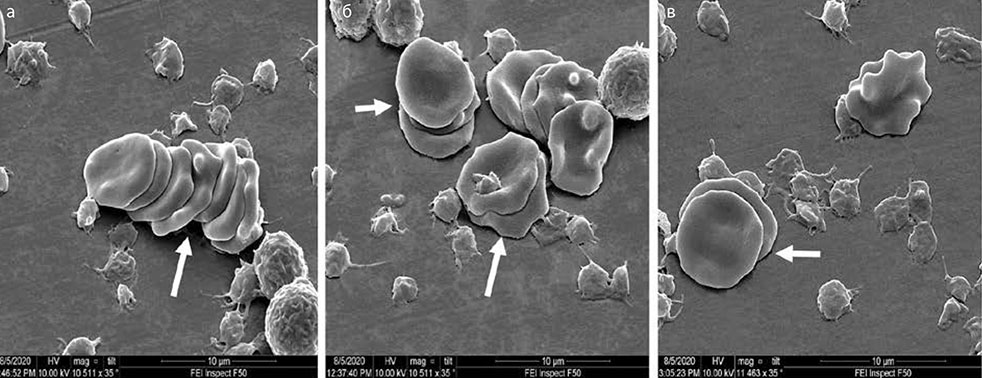
Рис. 9. Сладжи, образованные эритроцитами: а — циркулирующий в венозной крови больного сладж из 8 эритроцитов при
поступлении в клинику; б, в — более короткие сладжи у больных перед выпиской (ув. 10 тыс.) [13]

(ув. 25 тыс.) [13]
Группа ученых из Национального медицинского исследовательского центра кардиологии в Москве исследовала изменение картины клеточных элементов крови при поступлении больных в стационар и при выписке из него [13]. Электронная микроскопия крови больных показала, что при поступлении в стационар у всех пациентов в крови присутствовало значительное число поврежденных вирусом эндотелиальных клеток с многочисленными отверстиями на мембране. Размер отверстий был сопоставим с размером суперкапсида вируса SARS-CoV-2, что доказывало факт проникновения вируса в эндотелиальную клетку, где он реплицируется, после чего выходит в кровоток. Результат такого повреждения эндотелия — денудация сосудов, приводящая к увеличению их проницаемости, развитию отека тканей и воспаления, активации тромбоцитов и выраженному усилению тромбообразования.
Данное исследование показало, что при COVID-19 происходит образование эритроцитарных монетных столбиков (сладжей), способных закупоривать микрососудистое русло, нарушая снабжение тканей кислородом. В крови 80,6% больных как при поступлении, так и при выписке наблюдалась выраженная трансформация части эритроцитов в эхиноциты. Несмотря на нормализацию основных лабораторных параметров, характерных для воспаления, негативные эффекты, вызванные вирусом, сохранялись у части больных и при их выписке из стационара [13].
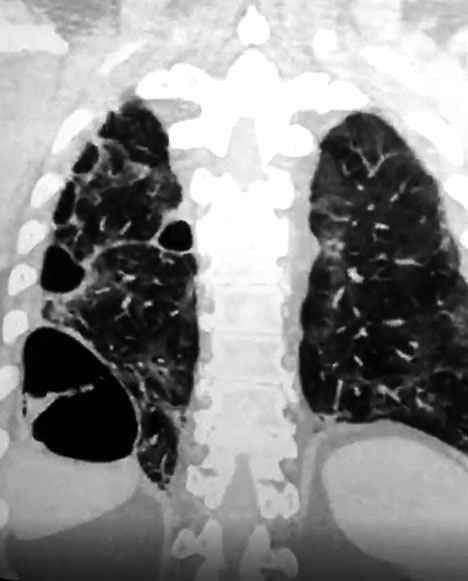
перенесшего в тяжелой форме COVID-19; буллезные
изменения на фоне выраженного фиброза легких [14]
С гибелью эндотелиоцитов происходит нарушение микроциркуляции, проявляющееся в замедлении кровотока по капиллярам, венулам и артериолам, что в свою очередь является причиной образования микротромбов. Коагулопатия при COVID-19 является другой причиной, усугубляющей гипоксемические расстройства. Нарастающая гипоксия приводит к гипоперфузии пораженных органов и тканей, формируется анаэробный тип метаболизма; концентрация лактата превышает физиологические параметры, отражая ишемию органов и тканей больного человека.
Врачи нередко задаются вопросом: почему не удается обеспечить вентиляцию легких для компенсации дыхательной недостаточности пациентам с COVID-19. На рис. 11 представлено персональное наблюдение за больным, перенесшим в тяжелой форме COVID-19; проводилась искусственная вентиляция легких в течение 10 дней. На КТ можно наблюдать множественные буллы, одна из них — гигантская. В просвете гигантской буллы виден обтурированный тромбом сосуд. Буллезные изменения развились на фоне выраженного фиброза легких: объемное уменьшение легочной ткани, множественные тракционные бронхиолоэктазы; процесс ремоделирования легких, вызванный фиброзным процессом и образованием множественных булл [14].
|
Патобиология COVID-19 включает четыре компонента:
|
Что же такое постковидный синдром? ВОЗ дает следующее определение: «Состояние, которое развивается после перенесенного заболевания COVID-19 у человека с подтвержденной молекулярно-биологическими методами инфекцией SARS-CoV-2. Постковидный синдром развивается к третьему месяцу от начала заболевания. Характеризуется симптомами, которые длятся в течение двух месяцев и не могут быть объяснены альтернативным диагнозом. Общие проявления включают: утомляемость, депрессию, одышку, когнитивную дисфункцию, а также возможно возникновение симптомов со стороны различных органов и систем человеческого организма».
Клинические фенотипы постковидного синдрома
Обобщение наблюдений за пациентами с постковидным синдромом, позволяет выделить некоторые группы больных.
Одну группу составляют пациенты, перенесшие тяжелую форму болезни, которым проводилась искусственная вентиляция легких, экстракорпоральная оксигенция в условиях реанимационного отделения. Состояние данной группы больных в постковидный период рассматривают как синдром постинтенсивной терапии, он является в некоторой степени аналогом посттравмаатического синдрома, описанного военными врачами. Одной из проблем этого особого типа больных является прогрессирующий фиброз легких в постковидный период.
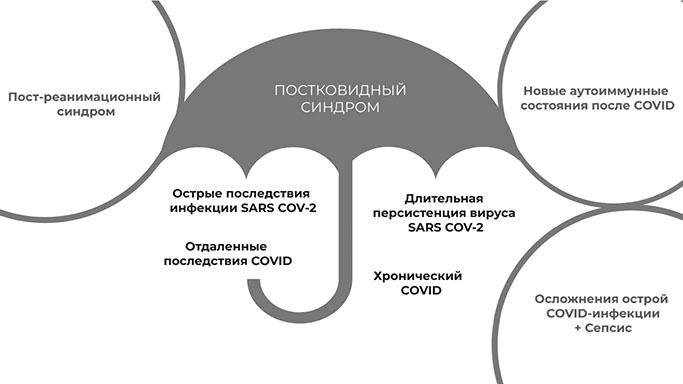

| Рис. 12. Клинические фенотипы постковидного синдрома | Рис. 13. Симптомы постковидного синдрома |
Другая группа — больные с новыми аутоиммунными состояниями после перенесенного заболевания COVID-19, ревматически подобными заболеваниями. Инфекция SARS-CoV-2 потенциально способна индуцировать обострение иммуновоспалительного процесса или развитие «новой» аутоиммунной патологии. В перечень постковидных синдромов входят артралгии, артриты, миалгии, васкулиты с поражением сосудов различного калибра, системная красная волчанка (СКВ), антифосфолипидный синдром, болезнь Кавасаки, а также целый ряд иммунологических маркеров (антифосфолипидных антител, антинуклеарных факторов и др.), характерных для широкого круга ревматических заболеваний [15].
Также можно выделить группу тяжелых пациентов, у которых наряду с симптомами COVID-19 развивались сепсис и септический шок. Большинство таких заболевших страдали от хронических заболеваний легких и сердца, сахарного диабета и артериальной гипертензии.
Фенотипом постковидного синдрома является затяжное течение COVID-19, диагностическим критерием данного состояния выступает персистенция симптомов вирусного заболевания сроком более чем 4 недели от начала болезни.
Наконец, под постковидным синдромом понимают персистенцию таких клинических проявлений болезни, как кашель, одышка, мышечные боли, снижение толерантности к физическим нагрузкам, депрессия и другие, которые наблюдаются на протяжении последних 3 месяцев от начала заболевания.
Литература
1. Shalk A. F., Hawn M. C. An apparently new respiratory disease of baby chicks // J. Am. Vet. Med. Assoc. 1931. № 78. P. 19.
2. Tyrrell D. A., Bynoe M. L. Cultivation of a novel type of common-cold virus in organ cultures // Br. Med. J. 1965. № 1. P. 1467–1470. DOI: 10.1136/bmj.1.5448.1467.
5. Lalchhandama K. The chronicles of coronaviruses: the bronchitis, the hepatitis and the common cold // Science Vision. 2020. № 20(1). P. 43–53. DOI: 10.33493/scivis.20.01.04.
4. Волынкина А. С., Ткаченко Н. О., Малецкая О. В., Скударева О. Н. и др. Крымская геморрагическая лихорадка: эпидемиологическая и эпизоотологическая ситуация в российской Федерации в 2022 г., прогноз заболеваемости на 2023 г. // Проблемы особо опасных инфекций. 2023. № 2. С. 6–12. DOI: 10.21055/0370-1069-2023-2-6-12.
5. Конкурентная борьба респираторных вирусов за место «под солнцем» [Электронный ресурс] // WhiteProduct. 2022. 20 октября. URL: ttps://white-product.com/info/news/konkurentnaya-borba-respiratornykh-virusov-za-mesto-pod-solntsem-2022/ (дата обращения: 13.09.2023).
6. Щелканов М. Ю., Попова А. Ю., Дедков В. Г., Акимкин В. Г., Малеев В. В. История изучения и современная классификация коронавирусов (Nidovirales: Coronaviridae) // Инфекция и иммунитет. 2020. № 10(2). С. 221–246. DOI: 10.15789/2220-7619-HOI-1412.
7. Walker M. Sniffing Out Where Virus First Strikes in COVID-19 [Electronic resource] // MedPage Today. 2020. August 19. URL: https://www.medpagetoday.com/infectiousdisease/covid19/88148 (accessed: 15.09.2023).
8. Ackermann M., Verleden S. E., Kuehnel M. et al. Pulmonary Vascular Endothelialitis, Thrombosis, and Angiogenesis in Covid-19 // The NEJM. 2020. № 383. P. 120–128. DOI: 10.1056/NEJMoa2015432.
9. Mak T. W., Saunders M. E. Cells and Tissues of the Immune Response // The Immune Response: Basic and Clinical Principles. Elsevier Inc, 2006.
10. Chen C., Haupert S. R., Zimmermann L., Shi X., Fritsche L. G., Mukherjee B. Global Prevalence of Post-Coronavirus Disease 2019 (COVID-19) Condition or Long COVID: A Meta-Analysis and Systematic Review // The Journal of Infectious Diseases. 2022. № 226(9). P. 1593–1607. DOI: 10.1093/infdis/jiac136.
11. Azzolini E., Levi R., Sarti R., Pozzi C., Mollura M., Mantovani A., Rescigno M. Association between BNT162b2 vaccination and Long COVID after infections not requiring hospitalization in health care workers // JAMA. 2022. № 328(7). P. 676–678. DOI:10.1001/jama.2022.11691.
12. Byambasuren O., Stehlik P., Clark J., Alcorn K., Glasziou P. Effect of covid-19 vaccination on long covid: systematic review // BMJ Med. 2023. № 2(1). P. e000385. DOI: 10.1136/bmjmed-2022-000385.
13. Бурячковская Л. И., Мелькумянц А. М., Ломакин Н. В., Антонова О. А., Ермишкин В. В. Повреждение сосудистого эндотелия и эритроцитов у больных COVID-19 // Consilium Medicum. 2021. № 23(6). С. 469–476. DOI: 10.26442/20751753.2021.6.200939.
14. Чучалин А. Г. Фиброз легких у больных, перенесших COVID-19 // Терапевтический архив. 2022. № 94(11). С. 1333–1339. DOI: 10.26442/00403660.2022.11.201943.
15. Особенности течения Long-COVID-инфекции. Терапевтические и реабилитационные мероприятия: Методические рекомендации // Терапия. 2022. № 1. Приложение. С. 1–147. URL: https://therapy-journal.ru/archive/article/41434 (дата обращения: 15.09.2023)



