 Александр Васильевич ГОРЕЛОВ,
Александр Васильевич ГОРЕЛОВ,
доктор медицинских наук, профессор, член-корреспондент РАН,
заместитель директора по научной работе Центрального
научно-исследовательского института эпидемиологии;
профессор кафедры детских болезней Первого Московского государственного
медицинского университета им. И. М. Сеченова
Второе десятилетие ХХI в. ознаменовалось появлением нового коронавируса SARS-CoV-2, поражающего человека и вызывающего инфекцию COVID-19.
Хронология событий:
- в конце декабря 2019 г. в городе Ухане провинции Хубэй центрального Китая были зарегистрированы первые случаи пневмонии неизвестного происхождения у местных жителей, связанных с местным рынком животных и морепродуктов Хуанань;
- 31 декабря 2019 г. власти Китая проинформировали ВОЗ о вспышке неизвестной пневмонии. С 22 января Ухань, а с 24 января — прилегающие к Уханю городские округа были закрыты на карантин;
- 30 января 2020 г. ВОЗ признала вспышку COVID-19 чрезвычайной ситуацией в области общественного здравоохранения, имеющей международное значение;
- 11 марта 2020 г. ВОЗ объявила, что вспышка приобрела характер пандемии;
- с 13 марта 2020 г. центром вспышки COVID-19 стала Европа.
|
Вирус SARS-CoV-2 — оболочечный одноцепочный РНК-вирус, относящийся к роду Betacoronavirus.
|
К настоящему моменту новый коронавирус SARS-CoV-2, относящийся к β-коронавирусам, хорошо изучен. Не вызывает сомнений, что это вирус природного происхождения и имеет ближайшее родство с SARS-CoV-1 или с MERS. Он не жизнеспособен в окружающей среде более 3–4 часов.
Коронавирусная инфекция охватила практически все страны, существует на всех континентах и подтверждено более 470 млн. случаев заболевания COVID-19 (на 03.2022).
Подтверждено также более 6 млн. летальных исходов, связанных с этой инфекцией за период пандемии.
Применительно к Российской Федерации, к марту 2022 г зарегистрировано более 17 млн. 600 тыс. случаев заболевания коронавирусной инфекцией. Летальные исходы, связанные с данным заболеванием, зафиксированы более чем у 365 тыс. человек.
Но для того, чтобы говорить о короновирусной инфекции, а не о группе респираторных инфекций в целом, необходимо говорить прежде всего о разработке подходов к диагностике данной инфекции. По образному высказыванию академика В. И. Покровского, «нет микроба — нет диагноза».
|
Лабораторная диагностика новой коронавирусной инфекции Организация лабораторной диагностики новой коронавирусной инфекции до особого распоряжения осуществляется в соответствии с требованиями СП 1.3.3118-13 «Безопасность работы с микроорганизмами I–II групп патогенности (опасности)». Для диагностики новой коронавирусной инфекции используют метод ПЦР-диагностики. Биологическим материалом для исследования является: материал, полученный при взятии мазка из носа, носоглотки и/или горла, промывные воды бронхов, полученные при фибробронхоскопии (бронхоальвеолярный лаваж), (эндо)трахеальный, назофарингеальный аспират, мокрота, биопсийный или аутопсийный материал дыхательных путей. Образцы для транспортировки должны быть транспортированы с соблюдением требований СП 1.2.036-95 «Порядок учета, хранения, передачи и транспортирования микроорганизмов I–IV групп патогенности». На сопровождающем формуляре необходимо указать наименование подозреваемой инфекции, предварительно уведомив лабораторию о том, какой образец транспортируется |
В настоящее время в Российской Федерации зарегистрировано беспрецедентное количество (более 500) различных тест-систем которые позволяют поставить диагноз:
- ПЦР-диагностика;
- мммуноферментный анализ (ИФА);
- иммунохроматографический анализ (ИХА);
- иммунохемилюминесцентный анализ (ИХЛА);
- проточно-инжекционный анализ (ПИА).
В январе 2022 г. Центральным научно-исследовательским институтом эпидемиологии Роспотребнадзора разработан и внедрен ПЦР-тест на две мишени в геноме SARS-CoV-2, позволяющий вторым этапом определять принадлежность возбудителя заболевания к той или иной генетической линии. При таком тестировании используются одновременно два участка с низким уровнем генетической изменчивости, если в одном фрагменте происходят изменения, за счет второго тест будет показывать верный результат. Является новой версией изотермической тест-системы. Используется полностью отечественная ферментная база.
Наука не стоит на месте, и в феврале 2022 г. в Центральном научно-исследовательском институте эпидемиологии Роспотребнадзора был разработан детектор на коронавирус, основанный на использовании системы CRISPR-Cas14 (в 2020 г. за открытие этой системы была присуждена Нобелевская премия E. Charpentier, J. Doudna).
Использование данной технологии позволяет выделять единичную копию SARS-CoV-2 и проводить диагностику у постели больного. Использование данных технологических платформ открывает новую историю диагностики не только короновирусной инфекции, но и всех вновь возникающих заболеваний.
Применение данной технологии позволяет обнаружить вирус SARS-CoV-2 при минимальной концентрации. Благодаря этому диагностировать COVID-19 можно будет на самых ранних стадиях заболевания. Такая технологии может стать основой системы, позволяющей быстро проводить диагностику прямо у постели больного. При этом производство тест-системы не требует высокотехнологичного оборудования, следовательно, затраты на ее внедрение будут невысокими при высокой оперативности получения результатов.
 В перспективе новая технология на основе системы CRISPR, разработанная учеными ЦНИИ Эпидемиологии Роспотребнадзора, может быть использована для разработки высокочувствительных и высокотехнологичных диагностических систем нового поколения, в том числе для разработки методов диагностики вновь возникающих инфекций. Данное изобретение ЦНИИ Эпидемиологии Роспотребнадзора зарегистрировано в Роспатенте РФ.
В перспективе новая технология на основе системы CRISPR, разработанная учеными ЦНИИ Эпидемиологии Роспотребнадзора, может быть использована для разработки высокочувствительных и высокотехнологичных диагностических систем нового поколения, в том числе для разработки методов диагностики вновь возникающих инфекций. Данное изобретение ЦНИИ Эпидемиологии Роспотребнадзора зарегистрировано в Роспатенте РФ.
Накопленные знания к настоящему моменту с уверенностью позволяют говорить о том, какая тест-система может быть использована в разных фазах инфекционного процесса. Но справедливости ради следует отметить, что наиболее точно установить диагноз во все фазы инфекционного процесса позволяет полимеразно-цепная реакция.
Для этого нужно использовать разные биологические среды, учитывая патофизиологию развития патологического процесса.
В настоящий момент в ЦНИИ Эпидемиологии Роспотребнадзора разработан патент «Способ оценки клинико-лабораторных данных» и получено свидетельство о регистрации программы на ЭВМ. Данный способ позволяет установить диагноз коронавирусной инфекции и установить клинические предикторы тяжелого течения этого заболевания.
С марта 2021 г. в Российской Федерации реализуется постановление правительства «Об утверждении Временного порядка предоставления данных расшифровки генома возбудителя новой коронавирусной инфекции (COVID-19)» [1], согласно которому на базе Центрального научно-исследовательского института эпидемиологии создана платформа для накопления базы данных о циркулирующих генетических линиях коронавируса. В эту платформу агрегированы данные по полногеномному и фрагментарному секвенированию, которые поступают изо всех учреждений, осуществляющих мониторинг возбудителя COVID-19, независимо от ведомственной принадлежности. К настоящему моменту создана отечественная web-платформа VGARuS для анализа генома SARS-CoV-2, интегрированная в международную базу данных, которая позволяет объективно судить в любой точке о циркуляции и преобладании того или иного генного варианта вируса.
Существует международный классификатор Pangolin, применяемый для классификации всех циркулирующих в мире штаммов SARS-CoV-2. Согласно этому классификатору, к первой категории — VOC — вариантам, вызывающим обеспокоенность (variant of concern), относятся
- Alpha («Британский», B.1.1.7);
- Beta («ЮАР», B.1.351);
- Gamma («Бразильский», P.1);
- Delta («Индийский-2», B.1.617.2 + AY);
- Omicron (B.1.1.529).
Во вторую категорию — VOI — варианты, вызывающие интерес (variant of interest), входят
- Lambda (C.37);
- Mu (B.1.621).
Третья категория — VUM — варианты, находящиеся под мониторингом (variant under investigation): AZ.5, C.1.2, Kappa (B.1.617.1), Iota (B.1.526), Eta (B.1.525), B.1.630, B.1.640. Это штаммы, имеющие единичные мутации, которые, возможно, приобретут свойства возбудителя и будут иметь пандемическое распространение.
Итак, эволюция короновируса или мутация — это привычная история развития эпидемического и пандемического процесса. В целом, применительно к SARS-CoV-2 регистрируется более 20 мутаций в год. Первая значимая мутация, затронувшая S-белок, с помощью которого короновирус адгезирует или прикрепляется к чувствительным клеткам человека и в первую очередь к АЦЕ-рецепторам, была зарегистрирована в середине февраля 2020 г. Полный геном вируса SARS-CoV-2 опубликован 10 января 2020 г.
Наглядно циркуляцию различных генных вариантов можно проследить на примере штамма Delta, вызвавшего наиболее тяжелые осложнения. В мире циркулировало более 100 генетических вариантов. Согласно отечественным данным, в нашей стране, как и в мире, наиболее часто встречались 10 линий. Каких-либо особых российских штаммов выделено не было.
Применительно к каждому генному варианту, очень важен мониторинг, или динамика распространения. Например, штамм вируса Omicron впервые был выделен с 1 по 8 ноября в ЮАР, 11 ноября — в Гонконге, 19 ноября — в Швеции, 20 ноября — в Англии и Израиле, 23 ноября — в Италии и Канаде, а 30 ноября он уже выявлялся в 17 странах на 4 континентах.
Филогенетический анализ очень важен для выясненеия происхождения любого штамма. Omicron имеет большее сродство к штамму Alpha или уханьскому, чем к штамму Delta. Если бы эволюционное развитие произошло от Delta, который сопровождался высоким уровнем летальности, госпитализаций, более тяжелым течением, сценарий развития пандемии был бы несколько иной. Полагают, что Omicron возник от уханьского штамма в организме иммуннокомпроментированного человека или группе иммуннокомпроментированных людей. Вторая теория приводит аргументы в пользу того, что именно штамм Alpha или уханьский перешел видовой барьер к домашним мышам, среди которых и произошла мутация, затем вновь осуществился переход к человеку и в итоге возник генный вариант Omicron.
Именно со штаммом Omicron связан подъем заболеваемости COVID-19 в 2022 г. Показатели четырех предшествовавших подъемов в Российской Федерации и в мире несопоставимы с аналогичными, связанными с указанным штаммом. Если на каждом предыдущем этапе развития пандемии суточная заболеваемость была выше 10, 20, 30, 50 тыс., то для штамма Omicron этот показатель превышал 220–240 тыс. случаев ежедневно.
|
Выявляемость геновариантов SARS-CoV-2 на территории Российской Федерации Геновариант Alpha был распространен на территории страны зимой 2021 г. Геновариант Delta распространился на территории страны во второй половине апреля 2021 г. и являлся доминирующим. Геновариант Beta встречался зимой 2021 г., в то же время, что и Alpha. Распространения не получил. Геновариант Gamma встречался в начале 2021 г., не получил заметного распространения. Геновариант Lambda (3) на сегодняшний день не представляет эпидемического значения на территории Российской Федерации. Геновариант Mu (8) на сегодняшний день не представляет эпидемического значения на территории Российской Федерации. Геновариант Omicron (2) обнаружен на территории Российской Федерации в рамках мониторинга среди пребывающих из-за границы граждан. |
COVID-19, зарегистрированных в Российской Федерации
на 10–11 неделях 2022 г.Caption
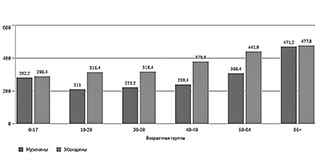
Возрастное и половое распределение заболеваемости штаммом Omicron на примере 2022 г. представлено на рис. 1.
В первой группе колонок мы можем видеть детские показатели, и очевидно, что впервые за всю историю развития пандемического процесса число и регистрация заболеваемости указанным штаммом среди детей сопоставимо со всеми другими возрастными категориями. Исключение составляют по-прежнему лица старше 65-летнего возраста, для которых даже в фазе снижения заболеваемости отмечаются наиболее высокие показатели как для мужчин, так и для женщин.
Первые случаи заболевания указанной разновидностью COVID-19 были зарегистрированы в РФ 4 декабря 2021 г. В настоящий момент циркулирует четыре ключевых линии Omicron: BA1, BA1.1, BA2, BA3 (рис. 2). В мире появились сообщения о том, что в регионах Юго-Восточной Азии доминирует разновидность штамма Omicron BA2.2 или Stealth (от англ.: скрытый, невидимый), который обуславливает некоторый подъем заболеваемости. Но объективности ради следует отметить, что островные страны Юго-Восточной Азии находятся в разных фазах эпидемического процесса. В этих государствах отмечается более редкая встреча с возбудителями заболеваемости и меньший охват вакцинацией, что приводит к подъему заболеваемости, который происходит в этих странах. В нашей стране в настоящий момент зарегистрированы единичные случаи В2.2 Stealth.
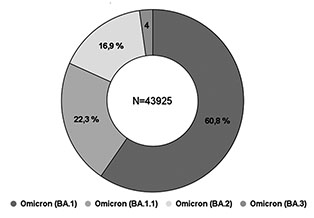
| Рис. 2. Структура геноварианта Omicron в образцах биоматериала с датой забора со второй недели 2022 г. |
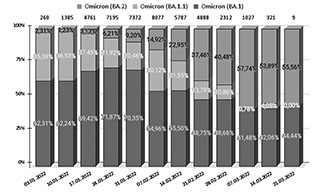
Рис. 3. Структура линии Omicron (B.1.1.529 + BA.*). Для образцов с датой забора биоматериала: 3 января – 21 марта 2022 г., по данным базы VGARus |
Обращаясь к данным российской базы VGARuS, мы отчетливо видим замещение одной генетической линии возбудителя коронавирусной инфекции на другую: снижается число и регистрация случаев заболеваний, обусловленных штаммом Omicron линии ВА1 и начинает преобладать линия ВА2, т. е. происходит смена генного варианта (рис. 3). Не наблюдается реального изменения клинической манифестации заболевания, что не может не радовать.
Что же будет дальше, после Omicron? По данным полногеномного и фрагментарного секвенирования, доля геноварианта Omicron в популяции SARS-CoV-2 на территории Российской Федерации на 11-й неделе 2022 г. достигла значения 100,0%, вытеснив Delta, Alpha и других представителей нового коронавируса. Дальнейшее развитие сценария событий представляется следующим образом: если не появится каких-либо других генетических вариантов SARS-CoV-2, будет наблюдаться постепенное снижение уровня заболеваемости. С некоторой периодичностью будут происходить подъемы (очаги, островки) заболеваемости, прежде всего среди лиц «наивных» или таких, у которых закончились сроки действия поствакцинальных антител. Следует помнить, что сроки ревакцинации установлены по временным рекомендациям РФ как после перенесенного заболевания, так и после проведенной вакцинации (ревакцинации) и составляют 6 месяцев.
Еще в ноябре 2021 г. в ЮАР была отмечена повторная заболеваемость короновирусной инфекцией в 15–20% [2]. То есть каждый 5-й, перенесший короновирусную инфекцию, вновь заболевал при встрече с Omicron.
Клинические и эпидемиологические черты Omicron. К настоящему моменту абсолютно точно установлено, что инфекция имеет высокую контагиозность. Она передается в 7 раз быстрее, чем другие возбудители COVID-19. Сократился инкубационный период: он составляет от нескольких часов до 2–5 дней. Эта особенность принципиально отличает Omicron, например, от уханьского штамма, для которого продолжительность инкубационного периода составляла 14 дней, в некоторых случаях 19–21 день.
В литературе появились данные о том, что в случае штамма Omicron ПЦР-тест чаще всего дает отрицательный результат в остром периоде заболевания. В данном случае ключевым моментом является техника забора биоматериала. Из-за того, что Omicron локализуется в основном в верхних дыхательных путях, более высокую чувствительность имеет забор материала с задней стенки глотки, что проводится в некоторых странах. В РФ проводится забор как из носовых ходов, так и с задней стенки глотки разными тампонами, затем все материалы помещаются в одну пробирку, т. е. способ забора биоматериала не имеет принципиального значения. Однако в случае Omicron важно, чтобы не было ложноотрицательных результатов, чтобы взятие биоматериала происходило с задней стенки глотки.
|
Эпидемиологические и клинические особенности мутации SARS-CoV-2 (Omicron) Симптомы, схожие с ОРВИ:
Особенности штамма Omicron:
|
По течению заболевание короновирусной инфекцией, обусловленной Omicron, в 97% случаев неотличимо от ОРВИ. В 80–85% случаев отмечаются классические симптомы острой респираторной инфекции, а у 10–17% отмечается бессимптомная форма заболевания, которая чаще всего выявляется при обследованиях контактных в очагах заражения либо при скриннингах, проводимых на промышленных предприятиях согласно предписаниям Роспотребнадзора (еженедельно 10% сотрудников подлежат плановому обследованию на выявление циркуляции SARS-CoV-2 и Omicron в частности). Так как на основании клинических данных не представляется возможным провести дифференциальную диагностику между Omicron и острыми респираторными вирусными инфекциями, при появлении симптомов респираторной инфекции необходимо незамедлительно обращаться за медицинской помощью и проводить соответствующее обследование.
В Российской Федерации с 2010 г. существует разработанная в Центральном научно-исследовательском институте эпидемиологии Роспотребнадзора тест-система ОРВИ-скрин, которая позволяет по одному мазку из носа и зева в одной реакции выделить 21 наиболее частый возбудитель респираторной инфекции, в том числе и короновирусной инфекции.
К характерным особенностям Omicron следует отнести наблюдающееся у 97% пациентов вовлечение в течение заболевания верхних дыхательных путей, которые являются по сути входными воротами инфекции. По сравнению с предыдущей манифестацией SARS-CoV-2 реже отмечается потеря обоняния, но при дебюте заболевания чаще наблюдается так называемый «мозговой туман», головная боль. Снижение аппетита, першение в горле и сухой кашель также являются ключевыми проявлениями данной инфекции. Следует отметить, что к постковидным явлениям при Omicron относят симптомы, связанные с тромбозом. Поэтому если после перенесенного заболевания у пациента продолжает наблюдаться слабость, вялость, длительный сухой кашель, першение и заложенность носа, необходимо обратиться за консультацией к соответствующему специалисту.
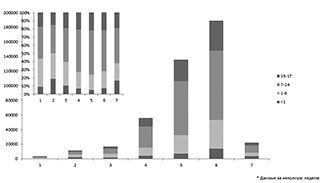
детей, больных COVID-19, в 2022 г.
Важным обстоятельством является то, что короновирусная инфекция, связанная с Omicron, наблюдается у детей с той же частотой, что и у взрослых. По этому поводу мы опубликовали серии работ [3]. В 2020 г. были некоторые сомнения относительно вовлечения детей в инфекционный процесс. Анализ данных на основании карт экстренных извещений свидетельствовал о том, что 2020 г. инфекция регистрировалась у 10–11% детей. В 2021 г. особенно с появлением Omicron частота регистрация короновирусной инфекции среди детей увеличилась и составила 23% (за год).
Заболеванию были подвержены дети всех возрастных категорий, но наиболее тяжело инфекционный процесс протекал у младенцев до 1 года и у подростков 14–18-летнего возраста. За первые два месяца 2022 г. доля короновирусной инфекции не уменьшилась и колебалась на уровне 19,2% (если взять всю заболеваемость за 100%).
Наиболее часто болеют маленькие пациенты до 6-летнего возраста. Это является некой особенностью протекания заболевания, вызванного штаммом Omicron, у детей.
С момента регистрации инфекции у каждого третьего ребенка отмечался диарейный синдром, часто встречались явления бронхиолита среди детей младшего возраста, ранее характерные для респираторно-синцитиальной инфекции и практически не наблюдавшиеся при короновирусной инфекции, обусловленной другими генными вариантами. Принципиальных отличий в частоте регистрации заболеваемости у мальчиков и девочек нами отмечено не было.
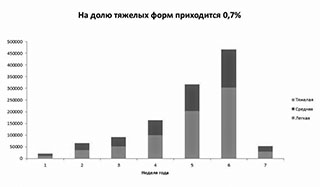
в динамике за первые 2 месяца 2022 г.
На долю тяжелых форм заболевания в динамике развития инфекционного процесса в 2020 г. приходилось 3,4%, в 2021 г. — 2,5%. Связано это в первую очередь с тем, что наблюдалась более легкая манифестация короновирусной инфекции. За первые 2 месяца 2022 г. на долю тяжелых форм приходилось 0,7% от всех заболевших (рис. 5). Но, учитывая масштабы распространения инфекции, обусловленной Omicron, в абсолютном выражении число тяжелых форм практически не изменилось.
Наиболее тяжелое протекание заболевания, вызванного штаммом Omicron, характерно для детей до 1 года с фоновыми заболеваниями (неврологические расстройства, хронические заболевания легких, включая астму, врожденные аномалии сердца и генетические нарушения), а также для лиц старше 60 лет с коморбидной или полиморбидной патологией.
В настоящий момент по мере накопления знаний наступила необходимость изменения клинической классификации коронавирусной инфекции. В 2020 г. ВОЗ предложила выделять следующие клинические варианты и проявления COVID-19:
- бессимптомная форма;
- острая респираторная вирусная инфекция (поражение только верхних отделов дыхательных путей);
- пневмония без дыхательной недостаточности;
- пневмония с острой дыхательной недостаточностью;
- острый респираторный дистресс-синдром;
- сепсис;
- септический (инфекционно-токсический) шок.
Собранные данные свидетельствуют о том, что помимо респираторных форм нередко встречается изолированное поражение, например, желудочно-кишечного тракта. В настоящий момент разработана тест-система, позволяющая выделять возбудителя из любой биологической среды, поэтому процент изолированного поражения ЖКТ колеблется от 10–25%, а в некоторых странах до 30%, и при этом важно подчеркнуть, что респираторных явлений практически не отмечается.
|
Гастроинтестинальная форма COVID-19
|
Синдром диареи при острой респираторной инфекции может сочетаться с респираторной патологией, с респираторными симптомами, но вместе с тем достаточно частым проявлением COVID-19 является изолированное поражение ЖКТ на разных этапах инфекционного процесса.
Синдром диареи и колит, на наш взгляд, может быть обусловлен
- прямым взаимодействием SARS-CoV-2 с эндотелием кишечника;
- прямым воздействием SARS-CoV-2 на микробиоту кишечника;
- бесконтрольным или бездумным использованием антибактериальных препаратов;
- токсическим воздействием на кишку лекарственными препаратами;
- инфекцией, связанной с оказанием медицинской помощи [5–8].
В последние годы появилось немало данных, говорящих о том, что короновирус может вызывать изолированное поражение центральной и периферической нервной системы, классическим проявлением может быть менингоэнцефалит.
COVID-19 принимает многие облики, потому что все рецепторы ACE2 представлены практически во всех органах и системах. На страницах журнала «Инфекционные болезни», входящего в международную базу данных Scorpus была развернута дискуссия о необходимости пересмотра классификации новой коронавирусной инфекции в свете накопленных данных [9]. В настоящий момент мы предлагаем к обсуждению следующую классификацию клинических форм коронавирусной инфекции:
- острая респираторная инфекция (поражение только верхних отделов дыхательных путей);
- пневмония без дыхательной недостаточности;
- пневмония с острой дыхательной недостаточностью;
- аносмия / паросмия / какосмия;
- гастроинтестинальная форма, гепатит;
- изолированные поражения ЦНС (менингит, менингоэнцефалит);
- малосимптомная форма / бессимптомная форма;
- сочетанные формы.
На наш взгляд сепсис, септический шок, инфекционно-токсический шок, ДВС-синдром (диссеминированного внутрисосудистого свертывания), тромбозы и тромбоэмболии необходимо рассматривать в качестве осложнений основного заболевания.
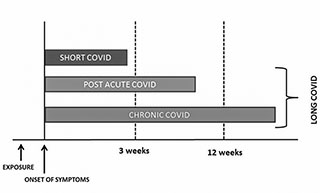
Национального института здравоохранения
и передового опыта (NICE) Великобритания,
декабрь 2020 г.
Отдельной проблемой стало постинфекционное состояние, или так называемые LONG COVID, POSTCOVID, а в настоящий момент предложено выделять и хронический COVID. Накоплены данные о том, что заболевание не заканчивается острым периодом, и в журнале «Терапия» (2022, № 1) были опубликованы предложенные и разработанные Национальным научным обществом инфекционистов и Российским научным медицинским обществом терапевтов методические рекомендации «Особенности течения LONG-COVID-инфекции. Терапевтические и реабилитационные мероприятия» [10].
Применительно к детям наиболее грозным синдромом был мультивоспалительный синдром. В апреле 2020 г. впервые появилось описание нового синдрома у детей, названного мультисистемным воспалительным («multisystem inflammatory syndrome in children» (MIS-C)) [11]. Его развитие, вероятно, связано с SARS-CoV-2. В ряде стран с высокой заболеваемостью (в Великобритании, Франции, Италии, США ) было отмечено, что в период снижения заболеваемости SARS-CoV-2 у детей и подростков увеличилась частота встречаемости синдрома Кавасаки, Кавасаки-подобного синдрома и мультисистемного воспалительного синдрома.
В период распространения штамма Omicron частота регистации мультивоспалительного синдрома или Кавасаки и Кавасаки-подобного синдрома значительно уменьшилась до единичных случаев. Под нашим наблюдением находилось более семидесяти детей с мультивоспалительным синдромом [12]. Необычность ситуации была связана с тем, что, по сути, острый период коронавирусной инфекции дети не замечали, а через две–три недели появлялись грозные симптомы, включающие несколько органов и систем, и требующие госпитализации — в 80% случаев в отделения реанимации и интенсивной терапии. В 20% случаев пациенты получали инвазивную механическую вентиляцию легких. Это является классическим проявлением патогенеза заболевания и иммунотромбоза. В 71% случаев в патологический процесс вовлекалось не менее четырех органов или систем, чаще всего желудочно-кишечный тракт (92%), сердечно-сосудистая система (80%), система кроветворения (76%), кожа и слизистые (74%) и органы респираторного тракта (70%). Четко установлены маркеры данного состояния у детей и взрослых, они изложены во временных методических рекомендациях.
|
При мультисистемном воспалительном синдроме, ассоциированном с перенесенной СOVID-19, у большинства пациентов наблюдаются следующие лабораторные и инструментальные данные:
|
Возвращаясь к Omicron, следует отметить, что при заболевании детей наиболее частой жалобой является длительное сохранение сухого кашля, сохранение болей в горле и неприятных ощущений слабости, вялости, что является, образно говоря, надводой частью айсберга. Спектр проявления постковидного синдрома весьма разнообразен, и необходим подход к реабилитации в зависимости от преобладающих жалоб по программам, разработанным соответствующими специалистами: неврологами, пульмонологами, врачами общей практики и реабилитологами. Накапливаются важные научные данные, говорящие о том, что в патогенетической основе развития постковида могут быть нарушения взаимодействия с микробиомом кишечника, в частности, в оси «легкие–кишечник» при коронавирусной инфекции [13]. В настоящий момент мы активно занимаемся изучением этого вопроса.
Что нового в лечении коронавирусной инфекции? На первых этапах развития инфекционного процесса COVID-19 летальность коррелировала с применяемой терапией, которую можно назвать, по сути, терапией отчаяния. Главной бедой было отсутствие специфических противовирусных препаратов, которые реально влияли бы на развитие инфекционного процесса и не позволяли бы развиваться цитокиновому шторму.
В настоящий момент применительно к лечению взрослых пациентов наметились позитивные сдвиги. Подходы к этиотропной терапии принципиально меняются, появились обнадеживающие данные по фактическому лечебному использованию специфических моноклональных антител для профилактики и предотвращения тяжелого течения заболевания применительно к генному варианту Delta. К сожалению, в случае генной разновидности Omicron моноклональные антитела практически потеряли свою терапевтическую нишу. Вместе с тем, получена доказательная база по позитивному безопасному использованию препаратов группы протеаз, которая действует на все РНК-содержащие вирусы, что нашло соответствующее отражение в клинических рекомендациях, регулярно утверждаемых Министерством здравоохранения РФ.
|
Принципы этиотропного лечения COVID-19 1. Прицельная (таргетная) этиотропная терапия, направленная на подавление / устранение / выведение вируса из организма. 2. Выбор этиотропного противовирусного средства базируется на доказанных и проверенных данных по эффективности и безопасности, регламентированных стандартизацией проведения клинических исследований для такой группы препаратов. 3. Только доказанная эффективность и безопасность являются основополагающими факторами для включения данного препарата во Временные методические рекомендации «Профилактика, диагностика и лечение новой коронавирусной инфекции» (Действующая версия 14 от 27.12.2021). |
Для этиотропной терапии COVID-19 Министерством здравоохранения рекомендованы следующие препараты:
- фавипиравир (таблетки, парентеральная форма),
- молнупиравир (капсулы),
- ремдесивир,
- синтетическая малая интерферирующая,
- рибонуклеиновая кислота (миРНК) [двуцепочечная],
- умифеновир,
- интерферон-альфа.
Для лечения детей из этиотропных препаратов в настоящий момент является доступными только умифеновир с двухлетнего возраста и интерферон альфа-2b.
Итак, задачи этиотропной терапии заключаются в подавлении/элиминации вируса (SARS-CoV-2), возбудителя COVID-19. Особое место занимают препараты ингибирующие вирусную РНК-полимеразу. Данная группа препаратов (фавипиравир, молнупиравир) показала свою эффективность против возбудителя COVID-19 и его многочисленных мутаций, а также против других РНК- вирусов (возбудителей ОРВИ), таких как вирус группа, включая А, В, С, сезонные штаммы и др.
Препарат Эсперавир (молнупиравир) включен в методические рекоменации по лечению COVID-19 в связи с доказанной клинической эффективностью. Данные исследований препарата свидетельствуют о более эффективном воздействии Эсперавир (молнупиравир) на динамику симптомов пациентов с COVID-19 (клиническое улучшение наступает в 2 раза быстрее), после 5-дневного курса терапии, по сравнению со стандартной терапией. Было показано, что препарат снижает риск госпитализации и ухудшения состояния пациентов, доказано отсутствие негативного влияния и побочных эффектов, которые послужили включением в рекомендации пятидневного курса терапии данным препаратов в терапии коронавирусной инфекции. Очень важным обстоятельством явилось то, что данный курс препарата у 88% пациентов к пятому дню способствовал элиминации коронавируса.
Применительно к детям основой базисной терапии являются рекомбинантные интерфероны [15]. При легких формах заболевания высокой противовирусной активностью, доказанной в опытах in vitro и in vivo, обладает, в частности, цетилпиридиния хлорид, который входит в состав комбинированных препаратов для взрослых и детей, широко используются для лечения респираторных инфекций [16].
Использование этих препаратов на ранних стадиях заболевания также способствует более легкому течению инфекционного процесса. В настоящий момент накапливаются фактические данные по расширению спектра прежде всего этиотропных препаратов, отрабатываются подходы к противовирусной специфической терапии.
Выводы
Разработка, внедрение новейших молекулярно-генетических методов диагностики новой коронавирусной инфекции (COVID-19), а также масштабирование производства позволили обеспечить потребность страны в массовом тестировании населения.
Мониторинг за эволюцией SARS-CoV-2, проводимый в Центральном научно-исследовательском институте эпидемиологии Роспотребнадзора, служит основой для принятия управленческих решений в области проведения лечебных, профилактических и противоэпидемических мероприятий по предотвращению дальнейшего распространения SARS-CoV-2, вектором для создания новых вакцин.
Накопленные данные о клинической манифестации болезни, особенностях ее течения у взрослых и детей позволили разработать и внедрить новые клинико-лабораторные дифференциально-диагностические критерии, поставить вопрос о пересмотре существующей классификации новой коронавирусной инфекции, включить в нее наряду с общепризнанными формами поражения легких, респираторного тракта, развитием бессимптомных и малосимптомных воспалительных процессов, формы изолированного поражения ЖКТ, нервной системы и ряда других органов, а так же доказать факт того, что сепсис, септический (инфекционно-токсический) шок; ДВС-синдром, тромбозы и тромбоэмболии следует рассматривать в качестве осложнений основного заболевания.
Хочется надеяться, что в ближайшее время коронавирусная инфекция, обусловленная SARS-Cov-2, станет не только сезонной, но приобретет черты управляемой инфекции. Для этого нужно соблюдение двух условий: одно из них — наличие вакцины, а второе — наличие специфических антикоронавирусных препаратов, при таких обстоятельствах угроза коронавирусной инфекции будет для человечества минимальной.
Литература
- Об утверждении временного порядка предоставления данных расшифровки генома возбудителя новой коронавирусной инфекции (COVID-19): поста Правительства РФ от 23 марта 2021 г. № 448 [Электронный ресурс] // Роспотребнадзор [сайт]. URL: https://www.rospotrebnadzor.ru/upload/t9q0kNv6z7jMAJIPluVd5hbDRyzWruxM.pdf (дата обращения: 23.12.2022).
- Pulliam J. R. C., van Schalkwyk C., Govender N., von Gottberg A. et al. Increased risk of SARS-CoV-2 reinfection associated with emergence of the Omicron variant in South Africa // medRxiv. 2021. December. doi: 10.1101/2021.11.11.21266068.
- Горелов А. В., Николаева С. В., Акимкин В. Г. Коронавирусная инфекция COVID-19 у детей в Российской Федерации // Инфекционные болезни. 2020. Т. 18. № 3. С. 15–20.
- Каннер Е. В., Каннер И. Д., Лапкин Н. М., Горелов А. В. Острые вирусные инфекции с сочетанным поражением респираторного и желудочно-кишечного тракта — бич современности // Педиатрия. Журнал им. Г. Н. Сперанского. 2021. Т. 100. № 6. С. 8–14.
- Zuo T. et al. Alterations in Gut Microbiota of Patients With COVID-19 During Time of Hospitalization // Gastroenterology. 2020. V. 159(3). P. 944–955. doi: 10.1053/j.gastro.2020.05.048.
- Smail S. W. et al. Inflammation, immunity and potential target therapy of SARS-COV-2: A total scale analysis review // Food Chem Toxicol. 2021. V. 150. P. 112087. doi: 10.1016/j.fct.2021.112087.
- Турчина М. С., Мишина А. С., Веремейчмк А. Л., Резников Р. Г. Клинические особенности поражения желудочно-кишечного тракта у больных с новой коронавирусной инфекцией COVID-19 // Актуальные проблемы медицины. 2021. Т. 44. № 1. С. 5–15.
- Ивашкин В. Т., Ющук Н. Д., Маев И. В. с соавт. Рекомендации Российской гастроэнтерологической ассоциации по диагностике и лечению Clostridium difficile-ассоциированной болезни // Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2016. Т. 26. № 5. С. 56–65.
- Горелов А. В., Плоскирева А. А., Понежева Ж. Б., Омарова Х. Г. с соавт. COVID-19 — многоликий Янус. К вопросу о классификации новой коронавирусной инфекции // Инфекционные болезни. 2021. Т. 19. № 4. С. 103–111.
- Особенности течения LONG-COVID-инфекции. Терапевтические и реабилитационные мероприятия. Методические рекомендации // Терапия. 2022. Т. 8. № 1 (приложение). С. 1–147. doi: 10.18565/therapy.2022.1suppl.1-147.
- Nakra N. A., Blumberg D. A., Herrera-Guerra A., Lakshminrusimha S. Multi-System Inflammatory Syndrome in Children (MIS-C) Following SARS-CoV-2 Infection: Review of Clinical Presentation, Hypothetical Pathogenesis, and Proposed Management // Children (Basel). 2020. V. 7(7). P. E69. doi: 10.3390/children7070069.
- Шалбарова Т. В., Сабинина Т. С., Мелехина Е. В., Музыка А. Д. с соавт. К вопросу о клинико-лабораторных особенностях мультисистемного воспалительного синдрома у детей, ассоциированного с SARS-CoV-2 // Вопросы практической педиатрии. 2021. Т. 16. № 6. С. 7–16.
- Новикова В. П., Хавкин А. И., Горелов А. В., Полунина А. В. Ось «легкие–кишечник» и COVID-инфекция // Инфекционные болезни. 2021. Т. 19. № 1. С. 91–96. doi: 10.20953/1729-9225-2021-1-91-96.
- Агейкин А. В., Горелов А. В., Усенко Д. В., Мельников В. Л. Экзосомы крови как новые биомаркеры инфекционных заболеваний // РМЖ. Медицинское обозрение. 2021. Т. 5. № 11. С. 744–748. doi: 10.32364/2587-6821-2021-5-11-744-748.
- Мелехина Е. В., Николаева С. В., Ильинская А. С., Понежева Ж. Б. с соавт. Рекомбинантные интерфероны в комплексной терапии новой коронавирусной инфекции // Инфекционные болезни. 2020. Т. 18. № 3. С. 41–46. doi: 10.20953/1729-9225-2020-3-41-46.
- Мелехина Е. В., Музыка А. Д., Понежева Ж. Б., Горелов А. В. Цетилперидиния хлорид в составе комбинированных препаратов для взрослых и детей в период пандемии COVID-19: подтвержденные возможности и перспективы // РМЖ. Медицинское обозрение. 2021. Т. 5. № 11. С. 728–736. doi: 10.32364/2587-6821-2021-5-11-728-736.



